-
- 작성자약학대학 관리자
- 작성일2026.03.05
- 조회수112
-
- 작성자약학대학 관리자
- 작성일2026.03.05
- 조회수95
-
최선 교수팀, 간암을 조종하는 ‘숨은 스위치 단백질’ TM4SF5 작동 원리 세계 최초 규명 최선 약학과 / 글로벌 AI 신약개발 연구센터 세포막단백질 TM4SF5의 독특한 이합체(dimer) 구조 및 형성 메커니즘 원자·분자 수준 규명 콜레스테롤 결합과 당화(N-glycosylation)가 이합체 안정화 및 암 신호 전달에 핵심임을 밝혀 세계적 다학제 분야 권위 국제학술지 게재 약학대학 약학과/글로벌 AI 신약개발 연구센터 최선 교수팀이 이정원 교수(서울대)와 이윤지 교수(중앙대) 연구팀과의 공동연구를 통해 간암과 섬유화 등 간질환을 조절하는 세포막단백질 TM4SF5 (Transmembrane 4 L Six Family Member 5)가 세포막에서 어떤 방식으로 움직이고 작동하는지 세계 최초로 규명했다. 간질환과 간암은 국내에서 발병률과 사망률이 모두 높은 중증 질환으로 지방간염과 간섬유화, 간경변을 거쳐 간암으로 악화되는 진행성 특징을 가진 데다, 현재 치료제의 효과도 제한적이다. 특히 간암은 최근 5년 생존율 개선 속도가 정체돼 있어 새로운 치료 전략의 필요성이 더욱 커지고 있다. 이 과정에서 세포막 단백질이 주고받는 신호는 간암의 성장과 면역 회피, 염증 반응에 직접 연관되는 중요한 기전으로 여겨진다. TM4SF5는 이러한 병리적 과정에 깊이 관여하는 ‘숨은 스위치 단백질’로서의 역할을 하지만, 그동안 정확히 어떤 구조로 존재하며 어떻게 작동하는지가 밝혀지지 않아 연구와 치료제 개발에 제약이 있었다. 연구팀은 단백질 서열 분석, AI 기반 구조 예측(AlphaFold3), 분자동역학 시뮬레이션, 돌연변이 실험을 종합해 TM4SF5의 작동 메커니즘을 정밀하게 분석했다. 그 결과, TM4SF5는 세포막에서 짝을 이뤄 이합체(dimer)로 움직이며, 특정 위치(N138, N155)가 당화(N-glycosylation)되는 과정을 통해 다른 단백질과의 결합을 조절하고, 콜레스테롤이 TM4SF5의 결합면에 자리잡아 구조를 더욱 안정화한다는 점도 밝혀냈다. 이는 TM4SF5가 간암 세포의 대사 재편성과 성장 신호 전달에 관여한다는 기존 연구를 구조적 관점에서 뒷받침하는 결과이다. 또한, TM4SF5가 기존에 유사하다고 여겨졌던 tetraspanin 계열이 아니라, 다른 단백질군인 CD20-like 패밀리와 더 가까운 독립적 진화 경로를 가진다는 사실도 밝혀냈으며, 이는 TM4SF5가 여타 단백질과 구별되는 독특한 구조와 기능을 지녔음을 의미한다. TM4SF5 이합체의 구조적 특징 및 핵심 인터페이스 모델 | TM4SF5 이합체 기반 신호전달 기전 이번 연구 결과는 TM4SF5의 구조적 특징, 이합체 형성, 당화(glycosylation), 콜레스테롤 결합이 실제로 기능 조절과 직결된다는 점을 최초로 입증한 것으로, 2019년 (IF 30.9), 2021년 (IF 13.3), 2024년 (IF 24.9) 등 세계적 권위지에 잇달아 발표해 온 TM4SF5 관련, 슈퍼컴퓨터를 활용한 분자모델링과 다학제적 융합 연구 성과이며, 향후 항체·저분자 억제제 등 TM4SF5를 겨냥한 치료제 개발을 가능하게 하는 기초 자료가 될 것이다. 연구팀은 “TM4SF5가 어떤 형태로 존재하는지 구조적 기전이 규명된 것은 치료 표적화를 가능하게 하는 매우 중요한 진전”이라며 “다년간의 융복합 공동연구 성과가 집약된 이번 결과는 간암뿐 아니라 다양한 대사성 간질환 연구에도 큰 도움이 될 것”이라고 기대를 밝혔다. 본 연구 결과는 과학기술정보통신부와 한국연구재단이 추진하는 선도연구센터사업(MRC), 바이오·의료기술개발사업(인공지능 활용 혁신신약 발굴 사업) 및 KISTI 국가슈퍼컴퓨팅센터(R&D혁신지원프로그램)의 지원을 받아 본교 약학과 최선 교수(공동교신저자), 윤상희 박사과정생과 서동혁 박사후연구원(공저자)이 참여하여 수행했다. 연구 결과는 다학제 분야 권위 국제학술지 (IF 13.0)에 12월 3일(수) 온라인으로 게재됐으며, 생물학연구정보센터(BRIC)의 ‘한국을 빛낸 사람들(한빛사)’에도 소개됐다. * 논문명 : 「Unique molecular architecture of N-glycosylated TM4SF5 dimer highlights evolutionary and structural divergence among small four-transmembrane protein families (DOI : 10.1016/j.jare.2025.11.066)」 * 한빛사 논문 정보 : https://www.ibric.org/bric/hanbitsa/researcher.do?mode=treatise-view&id=99632&authorId=29916&pager.offset=0&pagerLimit=10&srAuthorId=29916&beforemode=view#!/list * 관련 보도자료: https://www.ibric.org/bric/trend/bio-news.do?mode=view&articleNo=10009765#!/list
- 작성자약학대학 관리자
- 작성일2026.01.21
- 조회수333
-
김광명 교수 연구팀, Advanced Materials 학술지에 자가조립 펩타이드 기반 PROTAC 나노입자 (NanoTACs)를 이용한 야생형 및 변이 EGFR 표적 분해 치료 전략 발표 EGFR (상피세포 성장인자 수용체) 표적 치료제인 단일클론항체 (mAbs)와 타이로신 키나아제 억제제 (TKIs)는 암 치료에 널리 쓰이고 있으나, 약물 내성 (L858R/T790M 변이 등) 및 피부 발진과 같은 비표적 독성으로 인해 치료 효과에 한계가 있다. 또한, 기존의 저분자 화합물 기반 PROTAC (표적 단백질 분해 기술)은 낮은 세포 투과도와 종양 선택성 부족, 복잡한 합성과정 등의 문제로 임상 적용에 어려움을 겪어왔다. 이를 극복하고자 연구팀은 EGFR 결합 펩타이드 (EHGAMEI), 자가조립 펩타이드 링커 (FF), 그리고 E3 리가아제 결합 펩타이드 (ALAPYIP)로 구성된 자가조립 펩타이드 유도 PROTAC 나노입자 (NanoTACs)를 개발하였다. NanoTACs는 수용액 상에서 소수성 상호작용과 π-π stacking을 통해 약 144nm 크기의 균일한 구형 나노입자로 자가조립되며, 혈중 안정성을 유지한다. 특히 NanoTACs는 암세포에 유입된 후 '리소좀에 의한 직접 분해'와 리소좀 탈출 후 E3 리가아제에 의한 '프로테아좀 매개 분해'라는 이중 분해 기전을 통해 Wild-type뿐만 아니라 Mutant EGFR까지 효과적으로 제거하도록 설계되었다. 대장암(CT26) 및 내성 폐암(H1975) 마우스 모델에서 NanoTACs는 EPR 효과와 능동적 표적화를 통해 단분자 펩타이드 대비 2.24배 높은 종양 축적 효율을 보였으며, 종양 성장을 88.3% 억제하는 강력한 항암 효과를 입증하였다. 또한, NanoTACs는 기존 항체 치료제의 한계인 수용체 Recycling 기전을 차단하고, TKI 내성을 유발하는 돌연변이 EGFR까지 분해함으로써 약물 내성을 효과적으로 극복하였다. 동시에 정상 조직에 대한 독성은 나타나지 않아 높은 생체 안전성을 확인하였다. 본 연구는 자가조립 펩타이드 기반의 NanoTACs가 암세포의 Wild-type 및 Mutant EGFR을 동시에 표적하여 분해할 수 있는 강력한 플랫폼임을 증명하였으며, 기존 EGFR 표적 치료제의 내성 및 독성 한계를 극복할 수 있는 새로운 치료 전략을 제시하였다. 해당 연구 성과는 재료 분야의 세계적 권위지인 'Advanced Materials' 2025년 최신호에 게재되었다.
- 작성자약학대학 관리자
- 작성일2025.12.17
- 조회수708
-
김광명 교수 연구팀, Advanced Healthcare Materials 학술지에 cathepsin B 절단 독소루비신 프로드럭 나노입자를 이용한 종양특이 면역치료 전략 발표 독소루비신(DOX)은 강력한 면역원성 세포사멸(immunogenic cell death, ICD)을 유도하지만, 낮은 종양 선택성과 심장, 면역기관 독성으로 인해 고용량 투여 및 면역관문억제제와의 병용에 한계가 있다. 기존 나노약물전달체는 EPR 효과를 이용해 종양 축적을 높이려는 시도가 이루어졌으나, 실제 종양 축적률과 약물 봉입률이 낮아 정상조직 독성과 면역세포 소실을 충분히 줄이지 못한다. 이를 극복하고자 연구팀은 cathepsin B에 의해 선택적으로 절단되는 펩타이드(FRRG, FRRL, FRRLL, FRRLG, FRRGLL)를 DOX에 결합한 self-assembling 프로드럭 나노입자를 개발하였고, 입자형성 및 종양 축적이 가장 우수한 FRRL-DOX (CatB-NPs)를 최적 제형으로 도축하였다. CatB-NPs는 별도의 운반체 없이 자가조립되어 혈중에서는 안정하게 유지되다가, cathepsin B가 과발현된 종양 미세환경에서만 단계적으로 분해되며 DOX를 방출함으로써, 암세포에서는 핵 내 축적과 강한 세포사멸, ICD를 유도하고, 심근세포 및 수지상세포, T세포 등 정상세포와 면역세포에서는 독성을 크게 감소시키는 종양특이적 작용을 보인다. CT26 종양 마우스 모델에서 CatB-NPs는 free DOX 대비 혈중 체류와 종양 내 축적이 증가하고, 종양 성장 억제, ICD 지표 증가, 성숙 수지상세포와 CD8+ T세포 활성 증가를 동시에 달성하였다. 특히 anti-PD-L1 항체와 병용 시 종양 완전관해와 재도전 모델에서의 면역기억 형성이 관찰되었으며, 심장 및 비장 독성, 면역세포 감소는 현저히 줄어들었다. 본 연구는 cathepsin B 절단 펩타이드에 기반한 self-assembling DOX 프로드럭 나노입자가 암세포 특이적 ICD 유도와 면역세포 보존을 동시에 달성함으로써, 기존 DOX 기반 chemo-immunotherapy의 독성 한계를 극복할 수 있는 유망한 치료 플랫폼임을 제시하였으며, 관련 성과는 2025년 Advanced Healthcare Materials에 게재되었다.
- 작성자약학대학 관리자
- 작성일2025.12.08
- 조회수577
-
김광명 교수 연구팀, Advanced Drug Delivery Reviews 학술지에 초음파 감응 나노소재 기반 가스 전달 시스템의 최신 동향 논문 발표 종양 미세환경의 저산소증과 면역 억제성은 방사선·화학·면역치료의 효과를 떨어뜨리는 핵심 요인으로, 이를 극복하기 위한 산소(O2), 일산화질소(NO), 일산화탄소(CO), 이산화탄소(CO2), 황화수소(H2S) 등 치료용 가스 기반 전략이 주목받고 있다. 그러나 가스의 높은 확산성, 짧은 체류 시간, 전신 부작용 때문에 임상 적용에는 여전히 한계가 크다. 본 리뷰 논문은 이러한 문제를 해결하기 위한 대안으로, 초음파(ultrasound)를 자극원으로 활용하는 나노소재 기반 가스 전달 시스템(ultrasound-triggered gas delivery systems, UTGDS)의 설계 원리와 응용 현황을 체계적으로 정리하였다. 김광명 교수 연구팀은 초음파 조사 시 발생하는 cavitation, sonoporation, 열 효과를 이용해 가스 방출의 시간, 공간적 제어를 달성하는 전략을 중심으로, 지질 기반 마이크로버블 및 echogenic liposome, mesoporous/hollow silica 및 CaCO3, BaTiO3 등 무기 나노입자, PLGA 및 탄산 고분자 나노입자, 알부민, 페리틴, 가스 베지클 등 단백질 나노구조체, PFC 에멀전 및 MOF, 하이브리드 나노입자 등 다양한 플랫폼을 분류·비교하였다. 각 시스템의 가스 적재 방식, 초음파 조건, 영상화 가능성, 화학, 면역, 방사선, 광치료와의 병용 전략을 통합적으로 정리한 점이 특징이다. 또한 본 리뷰는 UTGDS의 임상 번역을 가로막는 과제로, 가스, 나노소재, 초음파 장치가 결합된 복합 시스템의 안전성 평가, 재현성 있는 대량 생산과 품질 관리, 종양 미세환경 이질성에 따른 맞춤형 설계, 장기 체내 잔류 및 분해산물 독성 검증 등을 제시한다. 본 논문은 초음파 감응 가스 전달 나노시스템이 종양 저산소증 극복과 약물 침투 향상, 영상-유도 정밀 치료를 동시에 달성할 수 있는 유망 플랫폼이며, 향후 난치성 고형암 치료의 새로운 패러다임을 제시할 수 있음을 강조한다.
- 작성자약학대학 관리자
- 작성일2025.12.08
- 조회수565
-
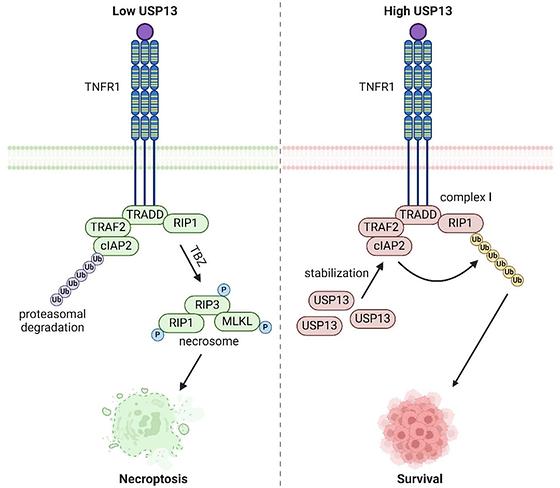
송은주 교수팀, 난치성 대장암의 치료 내성 해결할 핵심 단백질 발견 송은주 약학과 USP13- cIAP2 분해 조절 기전 규명… 새로운 항암표적 제시 국제 저명 학술지 Cell Death & Differentiation 게재 약학과 송은주 교수 연구팀이 기존 항암제에 반응하지 않던 난치성 대장암의 ‘세포 괴사 저항성’을 뒤집는 핵심 분자 기전을 규명하며 새로운 항암치료 전략을 제시했다. 이번 연구 성과는 생화학 및 분자생물학 분야 상위 2.5% 국제 저명 학술지 에 10월 22일(수) 온라인 게재됐다. 연구팀은 대장암 세포가 치료에도 살아남는 원인을 찾기 위해 세포 내 단백질 안정성을 조절하는 탈유비퀴틴화 효소 USP13의 역할에 주목했다. 그 결과, USP13이 세포사멸 억제 단백질인 cIAP2의 분해를 막아 대장암 세포 생존을 돕는 방패 역할을 한다는 사실을 밝혀냈다. USP13이 제거되면 cIAP2 단백질이 빠르게 분해되어 암세포가 네크롭토시스(necroptosis, 프로그램된 괴사성 세포사멸)에 더 취약해지며 기존 항암제의 효과 또한 크게 증폭되는 것으로 확인됐다. 이는 USP13이 대장암 세포의 생존을 매개하는 핵심 조절 인자임을 보여주는 중요한 발견이다. 대장암에서 USP13-cIAP2 축이 항암제 내성 및 세포 생존에 작용하는 분자 기전 모식도 연구팀은 임상 환자 데이터 분석에서도 USP13 발현이 높은 환자일수록 예후가 나쁘고 생존율이 낮아짐을 확인했다. 반대로 USP13을 억제한 세포와 동물 모델에서는 암 세포 성장이 급격히 감소하고, 항암제와의 병용 효과가 극대화됐다. 이러한 결과를 바탕으로 송은주 교수팀은 USP13을 직접적으로 억제하거나 cIAP2 단백질의 안정화를 방해하는 전략이, 기존 치료에 반응하지 않던 난치성 대장암 환자를 위한 새로운 맞춤형 치료 접근법이 될 수 있음을 제시했다. 송은주 교수는 “이번 연구는 암세포의 생존 신호를 정밀하게 조절하는 새로운 분자 기전을 규명함으로써, 치료 저항성 대장암의 한계를 극복할 수 있는 혁신적 치료 표적을 제시했다는 데 큰 의의가 있다”고 밝혔다. 이번 성과는 본교의 기초의학·생명과학 융합연구 역량이 국제적으로 인정받은 사례로, 암세포의 생존 기전을 분자 수준에서 규명한 점에서 학문적·임상적 파급력이 크다. 연구진은 향후 USP13 억제제 후보물질을 개발해, 난치성 대장암 환자 치료의 새로운 돌파구를 마련할 계획이다. 송은주 교수(교신저자), 김연정 박사(제1저자) 본 연구는 한국연구재단 중견연구자지원사업과 BK21 첨단바이오소재 인재양성 교육연구단, 교내 전임인력지원사업의 지원을 받아 진행되었으며, 실험에는 교육부 및 한국기초과학지원연구원(국가연구시설장비센터)의 지원으로 설립된 이화 신약개발연구코어센터의 첨단 연구장비가 활용되었다. 논문 바로 가기: https://www.nature.com/articles/s41418-025-01595-4
- 작성자약학대학 관리자
- 작성일2025.11.13
- 조회수704
-
- 작성자약학대학 관리자
- 작성일2025.11.04
- 조회수642
-
김광명 교수 연구팀, Advanced Healthcare Materials에 고용량 췌장암 치료용 리포좀 플랫폼 연구 발표 김광명 교수(이화여자대학교 약학과) 연구팀이 고용량 화학요법의 독성과 내성 문제를 동시에 해결할 수 있는 신개념 항암 리포좀 플랫폼을 개발하여, 국제학술지 Advanced Healthcare Materials에 연구 성과를 발표했다. 연구팀은 세포사멸을 억제하는 단백질(IAPs)의 발현이 높아 고용량 항암제에도 잘 반응하지 않는 췌장암에서, SMAC 모방 펩타이드와 독소루비신(DOX)을 결합한 프로드럭(SMAC-P-FRRL-DOX)을 설계하고, 이를 cathepsin B에 의해 종양 특이적으로 활성화되는 리포좀(Aposomes)으로 제형화하였다. 이 제형은 기존 리포좀과 달리, 고용량 정맥투여를 전제로 설계되었으며, 종양 내에서는 강력한 세포사멸을 유도하고, 정상 조직에서는 독성을 최소화하는 구조적 특성을 갖는다. KPC960 종양 모델 및 humanized NSG 마우스를 활용한 전임상 실험에서, Aposomes는 반복 고용량 투여에도 심장, 비장 등 주요 장기에서의 독성이 나타나지 않았으며, 종양 내에서만 선택적으로 활성화되어 우수한 종양 억제 효과를 보였다.특히, 기존 DOX에서 문제로 지적되던 심장 독성과 면역세포 억제 문제를 효과적으로 회피한 점에서 임상 전환 가능성이 높은 고용량 항암 플랫폼으로 주목받고 있다. 본 연구는 췌장암과 같은 고저항성 암종에서 고용량 치료의 구조적 한계를 극복할 수 있는 새로운 설계 전략을 제시한 것으로, 향후 다양한 항암제와의 적용 확장을 통해 고용량 화학요법의 치료 지수를 개선하는 정밀 약물전달 기술로의 발전이 기대된다.
- 작성자약학대학 관리자
- 작성일2025.08.05
- 조회수1203
-
김광명 교수 연구팀, Acta Pharmaceutica Sinica B학술지에에 광활성화 PROTAC 나노입자를 이용한 뇌종양 면역치료 전략 발표 최근 뇌종양 치료 분야에서는 종양 미세환경 내 면역 억제성을 극복하고 면역치료 반응을 유도하기 위해 다양한 접근이 시도되고 있으나, 여전히 면역관문억제제의 낮은 반응률과 면역세포 탈진, 그리고 약물의 혈관-뇌 장벽(BBB) 통과 한계 등이 임상 적용에 큰 제약으로 작용하고 있다. 이러한 한계를 극복하고자, 김광명 교수 연구팀은 광감각제와 PTP1B 표적 PROTAC을 cathepsin B 절단 펩타이드로 연결한 자가조립형 나노입자(PNPTP1B)를 개발하였다. 이 시스템은 기존의 운반체 없이도 π-π stacking을 통해 자발적으로 나노입자를 형성하며, 광역학치료와 단백질 분해 기전을 동시에 유도할 수 있도록 설계되었다. PNPTP1B는 뇌종양 진행 과정에서 BBB가 붕괴된 영역에 특이적으로 축적되고, cathepsin B에 의해 광감각제와 활성화된 PROTAC으로 효소적 분해된다. 이후 레이저 조사 시 광감각제에 의해 생성된 ROS와 PROTAC에 의한 PTP1B 분해가 시너지 작용을 일으켜, 면역원성 세포사멸을 유도하고, T 세포의 PD-1, Tim3 발현 억제를 통해 탈진을 회복시킨다. 그 결과, 골수 유래 수지상세포의 성숙과 종양 특이 T 세포의 증식 및 활성화가 촉진되어 종양 내 강력한 면역반응을 유도하였다. 본 연구 결과는 2025년 Acta Pharmaceutica Sinica B에 게재되었으며, 마우스 GBM 모델에서의 PNPTP1B 정맥 투여 후 약물의 종양 특이적 축적, T세포 재활성화, 완전관해, 재도전 모델에서의 면역기억 유도 등이 확인되었다. 특히 정위적 뇌종양 모델에서도 광역학치료와 병합된 PNPTP1B가 종양 축소, CD8⁺ T세포 침윤 증가, 탈진 마커 감소 등 우수한 치료효과를 보였고, 정상 조직에 대한 독성은 관찰되지 않았다. 이 연구는 광역학 치료와 PROTAC 기반 단백질 분해 기전을 통합한 혁신적인 치료 플랫폼을 제시하였으며, BBB 통과가 가능한 나노조립체를 활용한 정밀 면역치료 가능성을 입증한 중요한 성과로 평가된다. 향후 광전달 장치와의 결합을 통해 뇌종양을 포함한 난치성 암 치료의 새로운 패러다임을 제시할 수 있을 것으로 기대된다.
- 작성자약학대학 관리자
- 작성일2025.07.22
- 조회수1146